Koenzym Q10 – powstawanie, właściwości i zastosowanie w preparatach kosmetycznych
Autor: Urszula Gałka, Jan Ogonowski
Od ponad 2000 lat człowiek poszukuje sposobów na przedłużanie życia i nieśmiertelność. Średniowieczni jatrochemicy i alchemicy produkowali „eliksiry młodości” destylując, ekstrahując i macerując przeróżne rośliny, jady, tkanki zwierzęce i minerały. Powstawały w ten sposób substancje nazywane wówczas „piątą esencją”, „kamieniem filozoficznym” czy „eliksirem młodości”.
Podobnie i w dzisiejszych czasach współczesna medycyna poszukuje panaceum na zatrzymanie wciąż młodego, zdrowego i pięknego wyglądu. Stosowane w dzisiejszych czasach witaminy, minerały oraz inne mikroelementy, aktywne „bio-cząsteczki” dają starzejącym się komórkom elementy odżywcze niezbędne do prawidłowego funkcjonowania. Wzmagają w ten sposób procesy odnowy skóry (szczególnie w miejscach zmarszczek).
W 1957 roku w Laboratorium Badań Enzymatycznych Uniwersytetu w Wiscosin z mitochondrium komórki mięśnia sercowego wołu został wyizolowany żółty związek. W 1959 roku ten sam związek wyizolowała oraz opracowała jego budowę chemiczną grupa naukowców kierowana przez prof. Karla Folkersa. Dokładną strukturę tego enzymu ustalił zespół badaczy z Hoffman – La – Roche i Zakładu Chemii Nieorganicznej w Bazylei [1].
Badania nad koenzymem Q10 rozpoczęto blisko 40 lat temu. Uzyskane wówczas informacje dotyczące jego budowy i właściwości pozwoliły na zakwalifikowanie go do grupy związków posiadających właściwości utleniająco-redukcyjne, biorących udział w najważniejszym cyklu przemian metabolicznych, czyli tzw. cyklu Krebsa. Koenzym Q10 (forma zredukowana to pochodna hydrochinonu natomiast forma utleniona to ubichinon) jest przenośnikiem elektronów w łańcuchu oddechowym. W okresie badań prowadzonych nad tajemniczym związkiem okazało się, że jest on niezbędny do produkcji energii, bez której organizm nie może żyć.
Powszechność jego występowania w wielu narządach różnych gatunków zwierząt sprawiła, że określono go mianem ubichinon (ubitarius – wszechobecny). Obecnie na całym świecie miliony osób stosują preparaty zawierające koenzym Q, a dalsze badania wciąż rozszerzają zakres i możliwości terapeutyczne stosowania tego związku [1,2].
W skórze człowieka zawartych jest bardzo dużo enzymów, które są niezbędne do jej prawidłowego funkcjonowania. Enzymy są biokatalizatorami, substancjami białkowymi, które biorą udział w metabolizmie tkankowym. Z kosmetycznego punktu widzenia enzymy odgrywają bardzo ważną rolę w fizjologii skóry, m. in. rozkładają stare tkanki, wyłapują wolne rodniki.
W kosmetyce bardzo rzadko stosuje się enzymy w pierwotnej (czystej) postaci. Jednym z najnowszych, coraz częściej pojawiającym się w recepturach preparatów kosmetycznych jest koenzym Q, nazywany CoQ10 lub Q10.
POWSTAWANIE, WŁAŚCIWOŚCI I WYSTĘPOWANIE KOENZYMU Q
Ubichinony są substancjami krystalicznymi, nierozpuszczalnymi w wodzie, dość łatwo rozpuszczają się w rozpuszczalnikach organicznych. Koenzym Q10 to intensywnie żółta, rozpuszczalna w tłuszczach, a nierozpuszczalna w wodzie substancja. Ma specyficzny zapach. Jest substancją fotostabilną, ulega 10% degradacji przy 5 MED i 60% przy 10 MED. Wykazuje również właściwości termostabilne. Jest odporny na ogrzewanie pod ciśnieniem, dzięki czemu można go dość łatwo wprowadzić do receptur kosmetycznych. Pomimo dość dużej odporności, w temperaturze powyżej 50 st. C, a nawet już 35 st. C może dojść do jego uszkodzenia i zmiany jego właściwości [2,3]. Jego masa cząsteczkowa wynosi 863,34 g/mol, a wzór sumaryczny ma postać C59H90O4 [4].
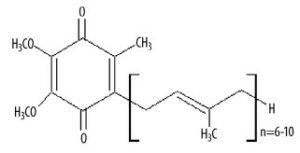
Koenzym Q10, nazwany również witaminą Q10, ubichinonem bądź ubidekarenonem. Początkowo przypuszczano, że koenzym Q10 ma strukturę steroidu, jednak obecnie wiadomo, że związek ten to 2,3-dimetoksy-5-metylo-6-poliizoprenylobenzo-1,4 benzochinon (rys.1). Jest zaliczany do szeregu homologicznego ubichinonów, związków będących pochodnymi 5-metylo-2,3-dimetoksychinonu [5].W przyrodzie spotyka się różne struktury zawierające zmienną liczbę reszt izoprenowych. Dla organizmu ludzkiego formą aktywną jest witamina Q o 10 resztach izoprenowych, stąd jego nazwa – koenzym Q10. Ubichinon wykazuje pewną analogię w budowie z witaminami K oraz E. Swoją budową przypomina także budowę plastochinonu wykrytego w chloroplastach.
U zwierząt występują homologi ubichinonu różniące się długością poliprenylowego łańcucha bocznego. Z drożdży oraz pleśni wyizolowano homologi ubichinonu zawierające łańcuch poliprenylowy zbudowany z sześciu (CoQ6), siedmiu (CoQ7) i ośmiu (CoQ8) reszt izoprenowych, natomiast u poszczególnych kręgowców (np. szczurów) oraz u ssaków stwierdzono obecność koenzymu Q9 i Q10 (tabela 1.) [6]
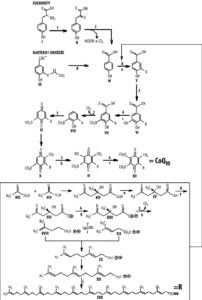
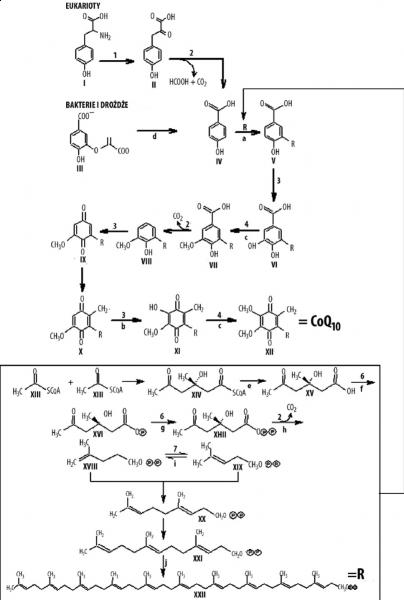
Koenzym Q10 jest syntezowany we wszystkich tkankach i komórkach organizmu w ilościach wystarczających do wypełniania swojej roli fizjologicznej. Sam proces biosyntezy koenzymu Q10 rozpoczyna się w retikulum endoplazmatycznym, natomiast kończy się w błonach aparatu Golgiego, skąd jest transportowany do innych organelli komórkowych. Koenzym Q10 może być syntezowany z różnych substancji. Bakterie i drożdże syntezują go z choryzmianu, organizmy eukariotyczne z tyrozyny, natomiast mikroorganizmy eukariotyczne mogą go syntezować zarówno z jednego jak i drugiego związku. Organizmy prokariotyczne oraz eukariotyczne, jako substratu do syntezy cząsteczki koenzymu Q10 potrzebują 4-hydroksybenzoesanu i grupy poliprenylowej. 4-hydroksybenzoesan powstaje w wyniku deaminacji tyrozyny do 4-hydroksyfenylopirogronianu (rys.2, II) i jego dekarboksylacji, natomiast grupa poliprenylowa syntezowana jest z acetylo-CoA (rys.2, XIII), który w wyniku kolejnych reakcji (redukcji, fosforylacji, dekarboksylacji i izomeryzacji) przekształca się w farnezylopirofosforan. Transprenylotransferaza wydłuża łańcuch farnezylopirofosforanu do dziesięcioczłonowego poliprenylofosforanu, z którego dziesięcioczłonowa jednostka poliprenylowa zostaje następnie przeniesiona na 4-hydroksybenzoesan, która jest katalizowana przez transferazę poliprenylową. Powstający w ten sposób 4-hydroksy-3-poliprenylobenzoesan po dekarboksylacji, kolejnych hydroksylacjach i metylacjach, przebiegających z udziałem S-adenozylometioniny, przekształca pierścień benzenowy w chinonowy, a to ostatecznie prowadzi do utworzenia cząsteczki koenzymu Q10 [7].
Intensywność procesu biosyntezy koenzymu Q10 jest uzależniona od wielu czynników. Do najważniejszych należą stres oksydacyjny (działanie zimna, hormonów tarczycy, wysiłek fizyczny) [6] i proliferatory peroksysomów. Najbardziej jednak istotną rolę w stymulowaniu biosyntezy koenzymu Q10 spełnia rodnik ubisemichinonowy (CoQ10H). Jednym z odkryć ostatnich badań naukowych jest również to, iż proces ten nasila się w obecności witaminy B2, B6, B12, a także kwasów foliowego (witamina B9) oraz pantotenowego (witamina B5) [7].
Ubichinony można otrzymać wyodrębniając je z ich naturalnych źródeł oraz w wyniku syntezy chemicznej, w wyniku kondensacji 2-metylo-5,6-dimetoksyhydrochinonu z odpowiednim poliizoprenoidem.
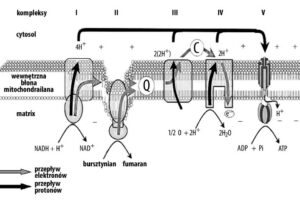
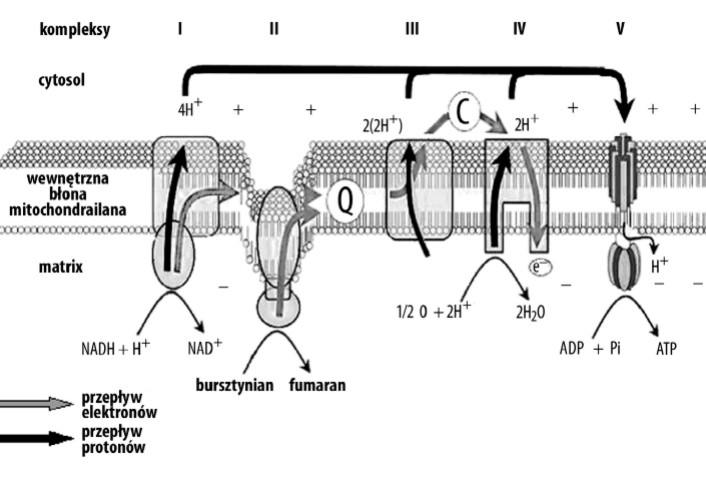
Koenzym Q10 jest niezbędnym ogniwem łańcucha oddechowego, jako podstawowy element odpowiedzialny za przemiany energetyczne w każdej żywej komórce. Bierze czynny udział w przenoszeniu elektronów. Jest niebiałkowym przenośnikiem odpowiedzialnym zarówno za transfer elektronów z kompleksu I lub II na kompleks III, oraz za przenoszenie protonów, które transportowane w poprzek błony tworzą tzw. gradient protonomotoryczny, a następnie są wykorzystywane do tworzenia ATP – wysokoenergetycznego związku fosforowego (adenozynotrifosforanu) (rys. 3) [1,3,7].
Występuje on również w błonach aparatu Golgiego, retikulum endoplazmatycznym, lizosomach, peroksysomach oraz w niewielkiej ilości w mikrosomach [7]. Koenzym wykazuje działanie stabilizujące błony komórkowe. Wynika to z faktu, iż wchodzi on w interakcje z białkami błonowymi, dzięki czemu błony są bardziej odporne na działanie szkodliwych czynników, oraz utrzymuje w odpowiednich ilościach substancje niezbędne do jej prawidłowego funkcjonowania (H2O, Mg2+, K+, Ca2+).
Sam mechanizm działania biologicznego ubichinonów polega na ich odwracalnej reakcji redukcji – utleniania. W żywym organizmie występują w równowadze dwie formy koenzymu O10; utleniona – ubichinon (CoQ10) oraz forma zredukowana – ubichinol (CoQ10H2) [3]. Wartość biologicznego potencjału wzorcowego dla formy utlenionej i zredukowanej koenzymu Q10 wynosi 0,1V [6].
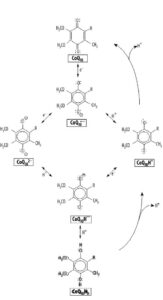
Rola koenzymu w transporcie elektronów wymaga ciągłego przekształcania się tych form, przy czym obie są aktywne [8]. Ubichinol działa jako przeciwutleniacz, ulega przemianie w koenzym Q10, który pod wpływem odpowiednich enzymów powraca do formy zredukowanej czyli ubichinolu (rys.4) [3]. Do enzymów tych należą: reduktaza NADH cytochromu b5 ,reduktaza NADPH cytochromu P-450, reduktaza NADP+ ferredoksyny, oksydoreduktaza NADH ubichinonu, a także oksydoreduktaza NADPH chinonu [7].
W organizmie możemy wyróżnić pośrednie formy koenzymu Q10, którymi są: rodnik ubisemichinonowy (CoQ10) oraz anionorodnik ubisemichinonowy (CoQ10H2)[3].
Rodnik ubisemichinonowy powstaje w wyniku działania wolnych rodników, np. alkilowego L*, nadtlenkowego LOO*, lub wodoronadtlenkowego HOO*na ubichinon (Reakcja 1). Anionorodnik ubisemichinonowy powstaje w reakcji deprotonacji rodnika ubisemichinonowego. Można go także otrzymać w wyniku reakcji ubichinonu lub ubichinolu
z anionorodnikiem ponadtlenkowym (Reakcja 2) [7].
 (1)
(1)
 (2)
(2)
Badania nad koenzymem Q wykazały, iż posiada on właściwości zarówno prooksydacyjne jak i antyoksydacyjne (rys.5).
Bezpośrednie działanie antyoksydacyjne wykazuje ubichinol. Mechanizm polega na oddaniu atomu wodoru przez ubichinol i utworzeniu rodnika ubisemichinonowego – CoQ10H*. Powstały rodnik może reagować z tlenem cząsteczkowym (Reakcja 3), bądź wchodzić w reakcje z innymi rodnikami (Reakcja 4), w wyniku czego powstaje koenzym Q10, który ze względu na brak atomu wodoru nie może pełnić roli antyoksydanta [7].
 (3)
(3)
 (4)
(4)
Występowanie w błonach biologicznych lipofilowego antyoksydanta alfa-tokoferol (witaminy E) ma związek z antyoksydacyjnym działaniem ubichinolu i rodnika ubisemichinonowego [7]. Koenzym Q10 redukuje rodnik alfa-tokoferolowy do alfa-tokoferolu, chroniąc go przed utlenieniem. Zwiększa to możliwości ochronne organizmu przed oksydacją lipidów błon komórkowych [1,3]. Działanie przeciwrodnikowe koenzymu Q10 nie jest uzależnione od występowania alfa-tokoferolu (witaminy E), natomiast ubichinol regenerując zredukowaną, biologicznie aktywną postać tokoferolu z jej postaci utlenionej lepiej chroni lipoproteiny przed oksydacją niż sam alfa-tokoferol [1,3,7].
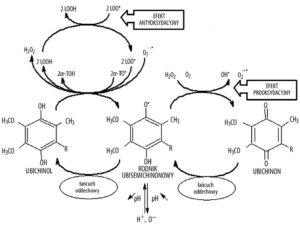 (5)
(5)
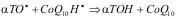 (6)
(6)
Koenzym Q10 oprócz właściwości antyoksydacyjnych posiada również właściwości prooksydacyjne. Działanie prooksydacyjne polega na tworzeniu w wyniku reakcji z tlenem reaktywnych form tlenu (HOO*) lub (O2-*), a ma je zarówno rodnik ubisemichinonowy (CoQ10H*) oraz anionorodnik ubisemichinonowy (CoQ10-*) [7].
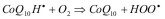 (7)
(7)
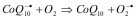 (8)
(8)
Ubichinon jest naturalnie produkowany przez wątrobę. W organizmie ludzkim wytwarzany jest z fenyloalaniny i tyrozyny. Bierze udział w wielu procesach przemiany materii. Wyniki badań potwierdzają, iż z wiekiem, przy nadmiernym obciążeniu psychicznym i fizycznym poziom koenzymu Q10 w organizmie znacznie się obniża. Zawartość koenzymu Q10 w poszczególnych narządach w danym wieku jest bardzo różna i można zaobserwować jego ubytek wraz z wiekiem (tabela 2). Jego niedobór może powodować zaburzenia w funkcjonowaniu wielu narządów m.in. serca, układu krwionośnego, odpornościowego oraz wielu innych o czym będzie mowa w rozdziale poświeconym zastosowaniu koenzymu [3].
Bogatym, a jednocześnie naturalnym źródłem koenzymu są produkty spożywcze. Najbogatsze w tą cenna witaminę są nerki, serca i wątroba, czyli organy o największym zapotrzebowaniu energetycznym. Jak wynika z danych zawartych w tabeli 3, zarówno mięso z renifera, serca wołowe jak i wieprzowe są bogate w koenzym Q, a jego masa waha się pomiędzy 113,3 – 157,9 ug/g surowego produktu, podczas gdy zawartość w rybach i innych produktach mięsnych wynosi 14,0 – 39,2 oraz 4,3 – 15,9 ug/g. Należy zatem powiedzieć, że mięso oraz ryby są produktami, które zawierają znaczne ilości tego cennego dla organizmu składnika. Zgodnie z prezentowanymi danymi warzywa, owoce, oraz nabiał również posiadają Q10 jednak w znacznie mniejszych ilościach [9,10].
Podsumowując, możemy stwierdzić, że bogatym źródłem koenzymu Q10 są produkty spożywcze na co dzień obecne w naszej diecie. Jego najbogatszym źródłem jest mięso oraz drób. Przeciętna zawartość tego ważnego suplementu diety wynosi 3-5 mg/dzień. Oprócz urozmaiconej diety bogatej w Q10, można go również dostarczać do organizmu w formie kapsułek dostępnych w aptekach oraz sklepach zielarskich.
Koenzym Q10 jest nietoksyczny oraz dobrze tolerowany przez organizm. Badania wykazały, że jego jednorazowe podanie nie wpływa na funkcjonowanie organizmu ani poszczególnych organów. Poprawa i zauważalne efekty występują po pewnym dłuższym czasie stosowania (kilkanaście dni). Produkty oraz zawartość w nich koenzymu Q10 zostały przedstawione w tabeli 3. Ze względu na to, iż rozpuszcza się on w tłuszczach oraz w alkoholu, miesza się go z lecytyną sojową i otrzymuje w postaci kapsułek. Bardzo dobrze wchłania się on z przewodu pokarmowego po jedzeniu, a nie na czczo. Samo wchłanianie jest powolne i niecałkowite. Maksymalna zawartość w osoczu występuje po 6-23 godzinach od podania doustnego, a następnie jest on rozprowadzony po całym organizmie i magazynowany głownie w wątrobie, nadnerczach, śledzionie, sercu, płucach oraz w nerkach [3,6].
METODY ANALITYCZNE POMIARU STĘŻENIA KOENZYMU
Pomiar zawartości koenzymu Q10 w płynach ustrojowych oraz narządach jest bardzo trudny. Powodem tego jest łatwe utlenianie ubichinonu podczas analizy. Poznane dotychczas metody pozwalają na pomiar całkowitej masy koenzymu Q10, czyli sumarycznej formy utlenionej i zredukowanej. Do oznaczeń tych potrzebne są metody analityczne bardzo czułe i selektywne. W konsekwencji wybór metod jest bardzo ograniczony.
Do najczęściej stosowanych metod analizy stężenia koenzymu Q10 w płynach ustrojowych należy chromatografia cieczowa HPLC z detekcją UV lub elektrochemiczną. Do pomiaru zawartości postaci zredukowanej, czyli ubichinolu (CoQ10H2) stosuje się detekcję elektrochemiczną, gdyż ta technika wykazuje dużą czułość. Natomiast pomiar zawartości ubichinonu (CoQ10) – czyli formy utlenionej koenzymu wykonuje się dzięki detekcji UV. Aby dokonać pomiaru stężenia obu form koenzymu Q10 jednocześnie stosuje się HPLC z detekcją kulometryczną, bądź tzw. kolumnę redukcyjną. Do najnowszych sposobów pomiaru należy technika sprzężonej chromatografii cieczowej i spektrometrii masowej – HPLC-MS. Pozwala ona na jednoczesny pomiar zawartości koenzymu Q10 oraz Q9 w organizmie. Do analiz zawartości koenzymu Q10 w materiale biologicznym stosuje się również metody spektroskopowe, m.in. elektronowy rezonans paramagnetyczny (EPR), magnetyczny rezonans jądrowy (NMR) oraz metody elektroanalityczne takie jak woltametria oraz metody spektrofotometryczne [6].
ZASTOSOWANIE KOENZYMU
Koenzym Q10 jest skutecznym zmiataczem wolnych rodników oraz wszelkich zalegających w organizmie trucizn. W połączeniu z witaminą E najefektywniej odtruwa komórki z toksyn, a także pomaga się ich skutecznie pozbyć. Zapobiega uszkodzeniu komórek, gdyż stanowi ich pierwsza linię obrony. Z wiekiem organizm wytwarza coraz mniej koenzymu. Do skutków należy spowolnienie procesów energetycznych i odnowy biologicznej komórki. Pomiary in vivo na skórze świni wykazały penetrację naskórka przez koenzym Q10. Dzięki dostarczeniu odpowiedniej ilość tego cennego związku, możliwa jest skuteczna ochrona przed procesami starzenia, m.in. likwidowanie już istniejących zmarszczek oraz regeneracja skóry [3]. Chroni on skórę przed niedotlenieniem. Pobudza jej metabolizm oraz regenerację. Przyspiesza jej odnowę biologiczną oraz skutecznie opóźnia procesy jej starzenia. Produkty zawierające w swym składzie Q10 chronią skórę przed zanieczyszczeniami ze strony środowiska oraz wolnymi rodnikami. Zwiększają zdolności obronne naskórka. Zwiększają jędrność skóry, działając na nią odmładzająco. Aplikacja koenzymu pozwala stymulować oddychanie komórkowe. Badania przeprowadzone po aplikacji tego związku potwierdziły, że stosowany na skórę przez kilka tygodni powodował zanik drobnych zmarszczek, znaczne wzrost jędrności, wilgotności oraz elastyczności skóry. Nastąpiło również rozjaśnienie przebarwień.
Badania dotyczące wykorzystania koenzymu Q10 potwierdzają możliwość jego szerokiego zastosowania w preparatach przeciwzmarszczkowych, ochronnych ale także w medycynie. Trwają obecnie badania nad możliwością wykorzystania go w preparatach kosmetycznych, jako naturalnego filtra przeciwsłonecznego o niskim ryzyku podrażnień [3,8,11].
Prekursorami zastosowania koenzymu Q10 w kosmetykach byli Skandynawowie. Od 1997 roku na rynku znajdują się preparaty kosmetyczne duńskiej firmy Vita-Care i szwedzkiej Fleur de Sante. W tym samym czasie wypuściła na rynek krem z ubichinonem firma Juvena oraz Nivea-Beiersdorf. Do znanych również na polskim rynku firm mających w swej ofercie specjalne linie kosmetyków należy firma Ziaja, Oceanic oraz laboratorium kosmetyczne dr Ireny Eris. Wiele znanych i cenionych laboratoriów działających pod marką Dior, Lancôme, Estée Lauder, czy klinik biotechnologicznych, takich jak Avene, Galenic, czy RoC, wykorzystuje w swoich produktach, obok innych komponentów, koenzym Q10 oraz jego dotleniające i regenerujące właściwości. Odpowiednia pielęgnacja skóry preparatami z aktywnym związkiem Q10 pozwala ograniczyć efekty działania rodników i starzenia się skóry. Nie należy jednak zapominać, że styl życia oraz właściwie skomponowana dieta uzupełniona suplementami koenzymu Q10 sprzyja zachowaniu młodości na dłużej.
Sam koenzym Q10 występuje w kremach oraz innych kosmetykach zwykle w połączeniu z innymi antyutleniaczami, m.in. z witaminą C, E, ekstraktami z Ginko – Biloba czy kwasem hialuronowym oraz jego solami.. Taki mariaż zapewnia synergię działania uzupełniających się związków. Te skuteczne połączenia występują w wielu kompleksowych liniach kosmetycznych znanych polskich i zagranicznych firm [1,12,13].
UWAGI KOŃCOWE
Podsumowując, opublikowane dane na temat badania wpływu koenzymu Q10 na skórę są bardzo obiecujące. Jego właściwości pozwalają stosować go, jako naturalny filtr przeciwsłoneczny, natomiast szeroki wpływ na redukcję zmarszczek pozwala na używanie go w kremach przeciwzmarszczkowych jako, skutecznego antyoksydanta. Jest składnikiem preparatów kosmetycznych wielu szanujących się firm kosmetycznych, których produkty przeciwzmarszczkowe są szeroko rozpowszechnione na rynku.
Spis literatury
- D. Rodowski, „Zastosowanie koenzymu Q10 w kosmetologii”, „Biuletyn kosmetologiczny”, (1998), 4,173-175
- A. Danysz, „Tajemniczy czynnik życia: Koenzym Q10”, „Beauty forum Polska”, (1998), 6, 25-26
- M. Sikora, „Ważne odkrycie kosmetyki Koenzym Q10”, „Chemia kosmetyczna i gospodarcza”, (2001), 12, 47-49
- http://www.sigmaaldrich.com/catalog/search/ProductDetail?ProdNo=C9538&Br…
- E A. Zejc, M. Gorczyca, „Chemia leków”, PZWL, Wydanie II, Warszawa, (2002)
- J. Drzewoski „Farmakologia kliniczna koenzymu Q10”, http://www.q10.pl/drzewoski.pdf
- Siemieniuk, E. Skrzydlewska, „Koenzym Q10 – biosynteza i znaczenie biologiczne w organizmach zwierząt i człowieka”, Zakład Chemii Nieorganicznej i Analitycznej AM w Białymstoku, „Postępy Hig Med. Dosw. (online)”,(2005), 59, 150-159\
- M. Sikora, „Antyoksydanty – ochrona dla preparatu kosmetycznego, walka ze starzeniem skóry”, „Rynek chemii gospodarczej i kosmetyków”, (2005), 7-8, 12-15
- Pirjo Mattila, Jorma Kumpulainen, „Coenzymes Q9 and Q10: Contents in Food and Dietary Intake”, ,,Journal of Food Composition and Analysis”, (2001), 14, 409-417
- Christine Weber, Anette Bysted, Gunhild Holmer, ,,Coenzyme Q10 in Diet – Daily Intake and Relative Bioavailability”, ,,Molec. Aspects Med”, (1997), 18, 251-254
- Frederick L. Crane, Placido Navas, ,,The Diversity of Coenzyme Q Function”, ,,Molec. Aspects Med”, (1997), 18, 1-6
- „Koenzym Q 10 – nowa substancja czynna w nowych kremach Nivea”, „Pollena”(1999), 7/43, 293
- http://www.lekka.pl/czytelnia/Koenzym,Q10,,4,534.html
*Prof. dr hab. inż. Jan Ogonowski, Instytut Chemii i Technologii Organicznej Politechniki Krakowskiej; mgr inż. Urszula Gałka, absolwentka Wydziału Inżynierii i Technologii Chemicznej Politechniki Krakowskiej
Tabela 1. Występowanie homologów koenzymu Q [6].
|
Organizm |
Rodzaj koenzymu Q |
|
Escherichia Coli |
Q8, Q9, Q10 |
|
Drożdże |
Q6, Q7 |
|
Grzyby |
Q6, Q7, Q8, Q9, Q10 |
|
Rośliny |
Q8, Q9, Q10 |
|
Bezkręgowce |
Q7, Q8, Q9, Q10 |
|
Kręgowce ( myszy, szczury ) |
Q9, Q10 |
|
Człowiek |
Q10 |
Tabela 2 .Zawartość Koenzymu Q10(mg/mg) w narządach w różnym wieku [1,3].
|
Narząd |
Wiek (w latach) |
||
|
19-21 |
39-43 |
77-81 |
|
|
Płuca |
6,0 |
6,5 |
3,1 |
|
Serce |
110,0 |
75,0 |
47,2 |
|
Śledziona |
32,8 |
28,6 |
13,1 |
|
Wątroba |
61,2 |
58,3 |
50,8 |
|
Nerki |
98,0 |
71,1 |
64,0 |
|
Trzustka |
16,1 |
12,2 |
8,5 |
Tabela 3. Zawartość Koenzymu Q10 w produktach spożywczych [9,10].
|
Grupy produktów zawierających CoQ10 |
Zawartość CoQ10 [ug/g] w świeżym produkcie |
Zapotrzebowanie CoQ10 [mg/dzień] |
|
Mięso, drób Mięso z renifera |
157,9 |
2,2-3,2
|
|
Serca wieprzowe |
126,8 |
|
|
Serca wołowe |
113,3 |
|
|
Wątroba wołowa |
39,2 |
|
|
Wątroba wieprzowa |
22,7 |
|
|
Wołowina |
36,5 |
|
|
Szynka wieprzowa |
20,0 |
|
|
Kurczak |
14,0 |
|
|
Jaja |
1,2 |
0,06-0,08 |
|
Ryby Śledź bałtycki |
15,9 |
0,4 |
|
Pstrąg |
8,5 |
|
|
Łosoś |
4,3 |
|
|
Warzywa i owoce Kalafior |
2,7 |
0,2-0,3 |
|
Ziemniaki |
0,5 |
|
|
Pomidor |
0,9 |
|
|
Marchew |
1,7 |
|
|
Ogórek |
0,1 |
|
|
Groch |
2,7 |
|
|
Zielony groszek |
1,8 |
|
|
Pomarańcza |
2,2 |
|
|
Jabłko |
1,3 |
|
|
Kiwi |
0,49 |
|
|
Czarna porzeczka |
3,4 |
|
|
Truskawki |
1,4 |
|
|
Mandarynka |
0,9 |
|
|
Nabiał Jogurt |
2,4 |
0,1-0,5 |
|
Ser edamski |
1,2 |
|
|
Ser Emmental |
1,3 |
|
|
Mleko (1,5%) |
0,1 |
|
|
Chleb żytni |
<0,17 |
|
|
Chleb pszenny |
<0,09 |
|
|
Olej rzepakowy |
63,5 |
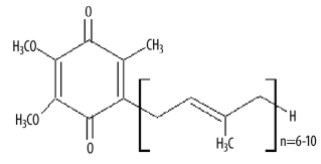
Rys.1. Koenzym Q10
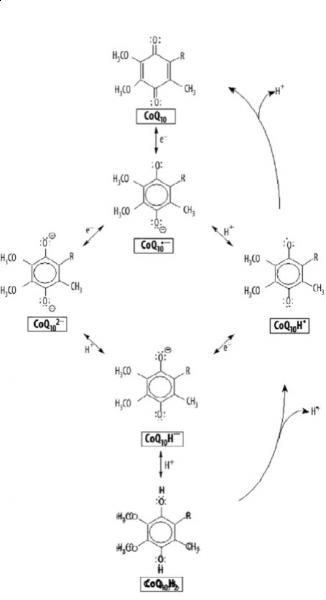
Rys. 4. Schemat przemian wolnorodnikowych koenzymu Q10 [7]
CoQ10 – ubichinon, CoQ10H2 – ubichinol, CoQ10-* – anionorodnik ubisemichinonowy
CoQ10H* – rodnik ubisemichinonowy, CoQ10H–, CoQ102- – aniony ubisemichinonowe
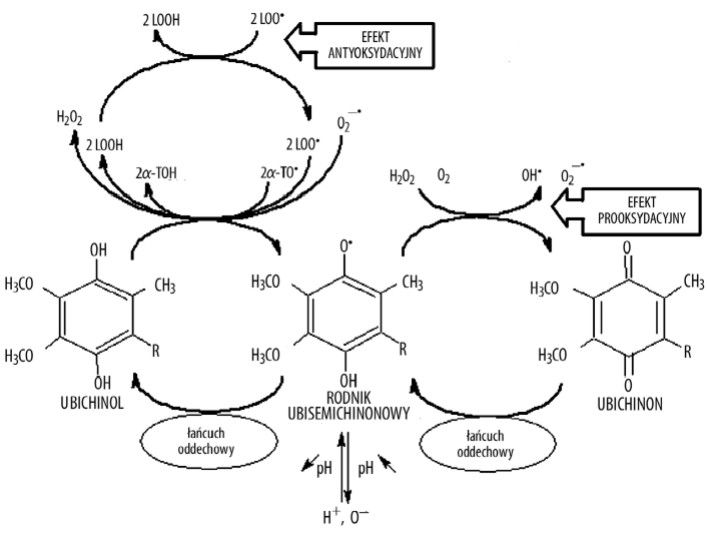
Rys. 5. Schemat działania anty- i prooksydacyjnego koenzymu Q10 [7]

